POLÍTICA DE PRIVACIDADE E COOKIES
Utilizamos alguns recursos para entender o que nossos clientes tem interesse e melhorar sua experiência. Ao continuar navegando, você concorda com nossa Política de Privacidade.
Entendi
Título do artigo: Regulação espacial de fibroblastos e células tumorais associados ao câncer por meio da administração de anticorpos biespecíficos responsivos ao pH para sinergia aprimorada de quimioimunoterapia: https://pubs.acs.org/doi/abs/10.1021/acsnano.4c13277
Título do periódico: ACS Nano
DOI: 10.1021/acsnano.4c13277
IF: 15.8
PMID: 40114589
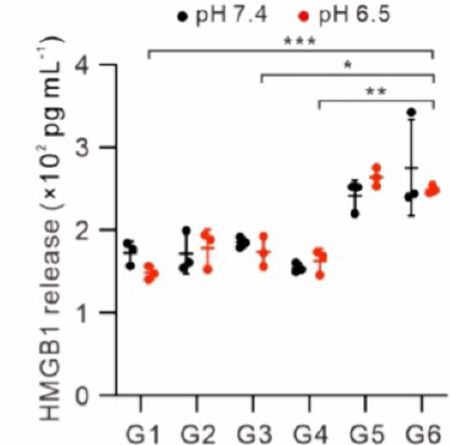
Resumo: A eficácia da quimioterapia é frequentemente comprometida por barreiras fisiológicas e um microambiente tumoral imunossupressor. Os fibroblastos associados ao câncer (FACs) contribuem significativamente para a reconfiguração da matriz extracelular (MEC) tumoral e para a supressão das respostas imunes, tornando-os alvos cruciais para intervenção terapêutica. Aqui, um sistema de entrega responsivo ao microambiente ácido do tumor que utiliza micropartículas derivadas de células tumorais (MPs) como carreadores para o agente quimioterápico doxorrubicina (DOX) e o anticorpo biespecífico YM101 direcionado a TGF-β e PD-L1 é desenvolvido (DOX@MPs-YM101) para regular espacialmente CAFs e células tumorais para eficácia quimioterápica aprimorada. DOX@MPs-YM101 alveja eficientemente tecidos tumorais e libera DOX@MPs e YM101 em resposta ao microambiente ácido do tumor. YM101 reprograma CAFs e reduz a MEC do tumor, facilitando o acúmulo tumoral e a penetração profunda de DOX@MPs-YM101. DOX@MPs são altamente internalizados em células tumorais, desencadeando morte celular imunogênica (ICD) e ativando a imunidade antitumoral mediada por células T CD8+. A reprogramação de CAFs por YM101 promove ainda mais o acúmulo de células T CD8+ e reduz o número de células imunossupressoras dentro dos tumores. Além disso, YM101 neutraliza eficazmente PD-L1 em células tumorais induzidas por DOX@MPs, restaurando a atividade das células T CD8+ e gerando memória imunológica antitumoral de longo prazo para prevenir a recorrência tumoral. Nossos resultados destacam o potencial de DOX@MPs-YM101 para aprimorar a quimioterapia no tratamento do câncer.
Palavras-chave: anticorpo biespecífico, fibroblastos associados ao câncer, quimioimunoterapia, morte celular imunogênica, micropartículas derivadas de células tumorais
Imunoensaio